前回の「溶ける量のたのしい不思議」の原子論的見方、つまり科学的な見方で実際の理科の問題(教員採用試験・高校入試レベル)を解いてみましょう。「科学、特に化学が大の苦手です」という方からの質問内容です。
みなさんも一緒に考えてみませんか。
問題
以下の物質の中で、60℃で溶けていた物質を20℃に下げた時、結晶として出てくる量が最も少ない物質は何か?
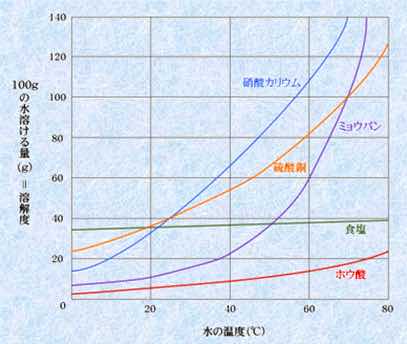
考え方
[硝酸カリウム]
グラフを見ると、硝酸カリウムは60℃の時110g 近く溶けています。それが20℃になる30gくらいしか溶けません。
とすると、溶けきれない80gは結晶として見える形で現れます。
硝酸カリウムの結晶は針の様な形をしているので、それがどんどん重なっていく様に見えます。

[ミョウバン]
ミョウバンは60℃でほぼ60g、20℃では10gくらいしか溶けませんから、50gくらい結晶として出てきます。硝酸カリウムが30gほどでしたから、かなりの量です。
ミョウバンの結晶は正八面体です。糸を垂らして結晶をつくると、正八面体の宝石の様な結晶がどんどん大きくなっていくので、自由研究などでも定番のものの一つです。コップをそのままにしておくとこんな感じで結晶が見えてきます。
この様な形でグラフを読み取っていくと、食塩が最も少ないことがわかると思います。⇦答え
はじめはまどろこしい感じがするかもしれませんが、一回はこうやって丁寧に考えて解いてみてください。
そのうちに「グラフのカーブがゆるやかなものだ」ということもイメージできると思います。だからと言って、子ども達に「ほら、カーブがゆるやかな方が答えなのよ」という様な教え方をすると、苦手な子や嫌いな子は、ますます・・・、ということにもなりかねません。
教員採用試験の合格を目指して方達向けに、少し関連することを書きましょう。
=食塩は塩化ナトリウムか?=
「〈食塩〉は科学的には〈塩化ナトリウム〉といいます」
という様に説明されることもあるので、混同してしまう人が多いのですが、化学的にいうと「塩化ナトリウム」という場合は、その純粋な物質です。「食塩」という場合はカリウム、マグネシウムなど、他のものも混ざった混合物です。
ですから厳密には違うのですけど、食塩の主成分(そのほとんど)は「塩化ナトリウム(NaCl)」なので、「ほぼ同じだ」という様に扱うこともある、ということで理解してください。
=アルカリ性物質と中性物質とを中和させてできるものは食塩か?=
違います。
中和させてできる物質を「塩」と書きますが「しお」とは読まず「えん」と呼びます。実にまぎらわしいですね。日本語を少し進化させて別な名称にした方がよいと思う一つです。
学校では酸性物質の代表として「塩酸」を使い、アルカリ性物質の代表として「水酸化ナトリウム」を使うので、結果として〈塩化ナトリウム〉ができます。つまり食塩の主成分なので、当然舐めると塩の味がするわけです。今では危険だということでなめされることはしませんが、わたしは何度も舐めたことがあります。
酸性の〈硫酸〉とアルカリ性の〈水酸化バリウム〉をちょうどよい割合で中和させると〈硫酸バリウム〉という「塩(えん)」ができます。これは食塩とはぜんぜん違う物質ですね。胃の検査でX線撮影する時に、苦しい思いをして「バリウム」を飲んだ人もいると思いますが、あれです。「塩(えん)」といってもいろいろあるのです。ですから、「酸性とアルカリ性を混ぜて中和させると〈食塩〉ができる」というのは間違いです。

